2017年将在美国上市的10大医疗设备 -凯发k8网页登录
新的一年到来,也意味着一连串新型医疗设备将在美国出现。被寄予厚望的产品包括糖尿病设备、新式经导管主动脉瓣,以及新型手术机器人系统。在此盘点今年患者期待看到的美国10大医疗设备。
no.1 波科公司的lotus edge

波科公司的新一代经导管主动脉瓣lotus edge预计将在2017年第四季度获得fda认证。这款新型瓣膜可以进行再定位和再回收,早期数据已经显示出瓣周漏和永久起搏器植入的低发生率。
reprise iii实验对lotus edge和美敦力的corevalve进行了比较,这些数据有望在2017年5月公布。这一实验数据将用于瓣膜21-、23-25、27-mm型号在第四季度获得fda批准。29-mm型号预计晚些获得批准。
截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
no.2 波科公司的vercise脑深部刺激系统
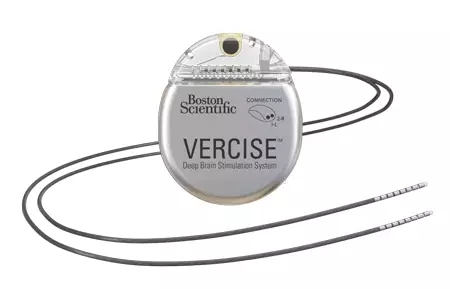
波科公司的vercise脑深部刺激(deep brain stimulation,dbs)系统正在针对帕金森综合征在美国进行试验。神经调节系统在欧洲已经用于包括帕金森病、特发性震颤、主要和次要肌张力障碍等适应症。
管理层述评波科公司2016年第三季度收入时,重申将在2017晚些时候在美国推出vercise。
截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
no.3 强生公司的onetouch via

用于胰岛素按需给量的onetouch via系统,早些时候,当这项技术属于calibra medical公司时,就获得了fda批准。目前,calibra medical是一家属于强生的糖尿病护理公司。该设备是一种可穿戴设备,用于胰岛素控制给量。onetouch公司及强生糖尿病护理公司北美区域高级管理人员bridget kimmel表示,2016年11月下旬,已经向fda重新提交了有关该设备更新生产流程的510(k)申请。她希望今年上半年onetouch via可以在美国市场面世。
截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
no.4 美敦力的minimed 670g系统
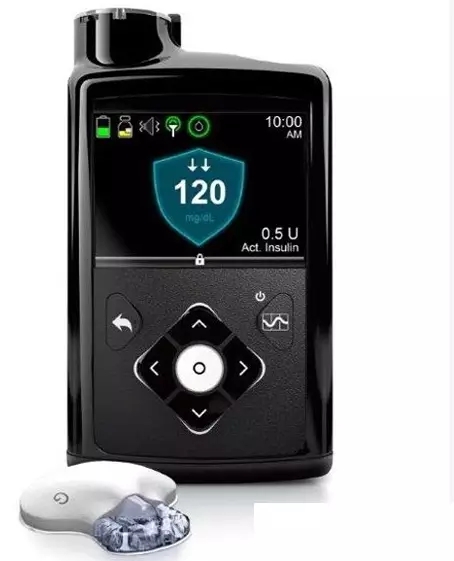
美敦力的minimed 670g是第一个用于胰岛素给药的混合闭环系统,被称为第一个人工胰岛素,2016年9月获得了fda批准。该系统旨在帮助患者在血糖水平合理范围之内获得最大化自由时间。
fda批准来得比预期的时间要早一些,美敦力计划2017年春季在美国市场推出这一系统。
no.5 美敦力的resolute onyx药物洗脱支架
药物洗脱支架(drug-eluting stent,des)巨头美敦力公司期望可以在最近一个财年(4月底)结束前在美国市场发布resolute onyx des。resolute onyx已经于2014年11月获得了欧洲ce认证,2016年2月增加了其他尺寸和适应症。截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
新的一年到来,也意味着一连串新型医疗设备将在美国出现。被寄予厚望的产品包括糖尿病设备、新式经导管主动脉瓣,以及新型手术机器人系统。在此盘点今年患者期待看到的美国10大医疗设备。
no.6 neuronix medical公司的neuroad治疗系统
据neuronews报道,neuronix medical的neuroad治疗系统预计在2017年拿到fda认证。这款设备旨在帮助阿尔茨海默病患者,将经颅脉冲磁刺激(transcranial magnetic stimulation ,tms))与认知训练相结合,改善患者的认知能力。
neuroad治疗系统已经在欧洲上市。截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
no.7 圣犹达公司的heartmate 3左心室辅助系统

圣犹达公司2015年10月收购 thoratec之后,仍继续对thoratec的heartmate 3左心室辅助技术进行持续开发。最新一代的heartmate 3左心室辅助系统(heartmate 3 left ventricular assist system ,lvas)已经获得ce认证,正在进行momentum 3 ide临床实验。2016年11月曾公布了该实验6个月内的跟踪数据。
目前在公开领域没有看到有关heartmate 3上市时间安排的消息,不过2016年2月该公司投资者曾表示,管理层承诺2016年下半年向fda提交短期数据。如果批准时间预计需要12个月,那么这款设备有望在2017年底获得fda认证。
截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
no.8 圣犹达公司可用于磁共振的icds和crt-ds

在2016年10月第三季度财报电话会议上,公司管理层向分析师表示,2016年第四季度将向fda提交mri安全性高压器件的文件。预计将在2017年上半年获得fda认证。
公司在2016年2月投资者报告日上曾表示,如果成功获得fda认证,那么代表磁共振安全的标志将可以用于现有的ellipse和fortify assura icds,以及quadra assura crt-d。
截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
no.9 史赛克用于mako系统的triathlon全膝关节
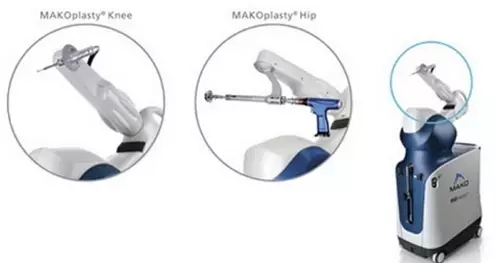
史赛克公司用于mako robotic系统的triathlon全膝关节(triathlon total knee)已经获得fda认证。
据2016年的报道,虽然fda在2015年8月已批准使用triathlon 全膝关节的mako系统,不过公司决定推迟到2017年再让产品上市,目的是为了优化患者体验。预计在2017年春季会隆重发布。
no.10 transenterix公司的senhance外科机器人系统
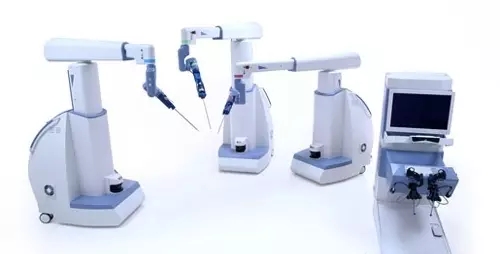
transenterix 公司的关注点从surgibot系统转向senhance外科机器人系统(之前命名为alf-x系统)。据报道,该产品的可用性研究已经完成,该公司计划在2017年初提交510(k)文件。
预计2017年senhanc将获得fda认证。截止2017年1月4日,这款产品尚未获得美国fda监管部门的批准或认可。
【来源: 科讯医疗网】

相关阅读
- 国内血管介入手术机器人赛道迎来“黄金时段”2022-11-02
- 支气管镜手术机器人开启肺部疾病诊疗赛道新篇章2022-03-02
- 最新排名出炉:2020全球顶级医疗企业top102021-02-05
- 21省耗材带量采购:美敦力、雅培、微创、乐普…2021-01-14
- 知名械企分食170亿市场:美敦力、史赛克、威高...2021-01-12






