近期20批医械召回,19品牌上榜! -凯发k8网页登录
11月7日,上海药监局发布20起医疗器械产品召回公告。
此次召回包括2项i级召回,11项ii级召回,7项iii级召回。其中,2项i级召回涉及的分别为库克的亲水涂层导丝和奥林巴斯的电子十二指肠镜。
此外,此次实施主动召回的有2家为国内医疗器械企业的国产产品。
1、奥林巴斯贸易(上海)有限公司
生产企业:奥林巴斯医疗株式会社
召回产品:电子十二指肠镜
召回原因:公司收到来自美国市场关于电子十二指肠镜发生病人感染病毒的投诉信息。经调查,这可能与电子十二指肠镜清洗消毒不彻底有关。
销售数量:在中国销售数量为12件。
召回级别:ⅰ
2、宾得医疗器械(上海)有限公司
生产企业:hoya株式会社
召回产品:电子十二指肠内窥镜
召回原因:部分电子十二指肠镜结构复杂,如果未能按照使用说明书指示进行清洗和消毒,会导致污染未能及时被清除,增加病人感染风险。
销售数量:在中国销售数量为55
召回级别:ⅱ
3、索灵诊断医疗设备(上海)有限公司
生产企业:diasorin inc。
召回产品:雌二醇测定试剂盒(化学发光免疫法)
召回原因:企业发现,氟维司琼可能与雌二醇测定试剂盒发生交叉反应,导致雌二醇检测结果假性升高。
销售数量:在中国销售数量为823
召回级别:ⅱ
4、通用(上海)医疗有限公司
生产企业:nevdel sas
召回产品:跟腱缝合导向器
召回原因:企业发现,涉及产品的无菌外包装可能无法保证在声称的灭菌有效期内保持其密封的完整性,影响产品内包装外表面保持无菌。
销售数量:在中国销售数量为142
召回级别:ⅲ
5、眼力健(上海)医疗器械贸易有限公司
①生产企业:abbott medical optlcs inc
召回产品:聚丙烯酸脂类后房型人工晶状体
销售数量:在中国销售数量为2
召回级别:ⅱ
②生产企业:abbott medical optlcs inc
召回产品:折叠式后房丙烯酸人工晶体
销售数量:在中国销售数量为4。
召回级别:ⅱ
召回原因:企业发现一台检验设备故障,导致部分人工晶状体在放行前未进行全部项目检查。这可能导致贴有错误标签的产品被放行,使用错误标签的人工晶状体可能导致潜在的非预期的术后屈光不正。
6、罗氏诊断产品(上海)有限公司
生产企业:roche diagnostica gnbh
召回产品:全自动气血、电解质和生化分析仪
召回原因:企业发现,涉及产品在检测新生儿血液样本时,可能会由于样本吸入测量池时延迟或样本未完全吸入,导致后续分析软件无法正确处理,进而得到错误偏低的新生儿胆红素检测结果。
销售数量:在中国销售数量为488
召回级别:ⅱ
7、飞利浦(中国)投资有限公司
生产企业:philips medical systems(cleveland),inc
召回产品:x射线计算机体层摄影设备、x射线计算机断层摄影设备
召回原因:企业发现在执行高分辨率头部扫描时,所重建的图像可能会出现图像质量降质。
销售数量:在中国销售数量为118
召回级别:ⅲ
8、强生(上海)医疗器材有限公司
生产企业:blosense webster(israel)ltd
召回产品:电生理导航系统
召回原因:发现有两个特定批次产品可能存在包装混淆,导致产品实际尺寸与包装标识不一致。
销售数量:在中国销售数量为54。
召回级别:ⅱ
9、施乐辉医用产品国际贸易(上海)有限公司
生产企业:smith & nephew,inc
召回产品:半髋关节假体组件
召回原因:由于生产过程中的错误,受影响产品的卡环沟槽位置尺寸超出产品设计要求,可能影响产品正常使用。
销售数量:在中国销售数量为1001
召回级别:ⅱ
10、碧迪医疗器械(上海)有限公司
生产企业:becton,dickins on and company
召回产品:动脉采血器
召回原因:公司发现部分产品无菌包装开裂,不能保证产品无菌。公司主动召回相关产品,通知相关单位收回受影响产品。
销售数量:在中国销售数量为19500
召回级别:ⅱ
11、库克(中国)医疗贸易有限公司(变更召回等级)
生产企业:cook incorporated
召回产品:亲水涂层导丝
召回原因:公司将亲水涂层导丝召回等级由二级升级为一级
销售数量:在中国销售数量为331
召回级别:ⅰ
12、柯惠医疗器材国际贸易(上海)有限公司
生产企业:covidien 11c
召回产品:呼吸回路
召回原因:公司发现实际进口到中国的呼吸回路产品与当时注册产品存在部分材质上的差异,不符合法规要求。
销售数量:在中国销售数量为11
召回级别:ⅲ
13、迈柯唯(上海)医疗设备有限公司
生产企业:maquet gmbh
召回产品:手术床系统
召回原因:公司发现制造适配器的材料未能达到公司规定的要求,不符合产品设计强度要求,影响患者使用安全。
销售数量:在中国销售数量为3
召回级别:ⅲ
14、贝朗医疗(上海)国际贸易有限公司
生产企业:b.braun melsungen ag
召回产品:一次性使用连续腰麻导管套件
召回原因:公司内部检测发现涉及产品的聚氯乙烯膜可能有空隙,影响无菌屏障系统。公司决定召回相关产品,向用户发出通知,冻结库存产品,回收客户未使用产品。
销售数量:在中国销售数量为5800
召回级别:ⅱ
15、贝克曼库尔特商贸(中国)有限公司
生产企业:beckman coulter,inc
召回产品:总铁结合力样本预处理柱试剂盒
召回原因:企业发现,总铁结合力样本预处理柱试剂盒的注册证、中文说明书和中文标签中的存储温度与英文标签中标注的存储温度不一致。
销售数量:在中国销售数量为3179
召回级别:ⅲ
16、飞利浦(中国)投资有限公司
生产企业:phiiips medical systems
召回产品:病人监护仪
召回原因:当本地设置为“报警开启”的出厂默认设定修改后,涉及产品将禁止ecg报警生成并传输至philipsintellivue信息中心piicix,并且piicix上不会显示ecg报警已禁用。
销售数量:在中国销售数量为150
召回级别:ⅱ
17、伯乐生命医学产品(上海)有限公司
生产企业:bio-rad laboratories,inc
召回产品:凝血质控物
召回原因:凝血质控物水平1,可能无法满足说明书上所示的开瓶后存放在2-25度的要求。
销售数量:在中国销售数量为3607
召回级别:ⅲ
18、上海卫康光学眼镜有限公司
生产企业:上海卫康光学眼镜有限公司
召回产品:软性亲水接触镜
召回原因:企业收到《国家医疗器械抽验产品检验结果送达告知书》,涉及产品“总直径”不合格。
销售数量:在中国销售数量为1644
召回级别:ⅲ
19、捷迈(上海)医疗国际贸易有限公司
生产企业:zimmer spine
召回产品:椎间融合器辅助工具
召回原因:产品说明书所列的清洗和去污方法,不能保证产品彻底清洗和去污,可能导致病人感染危险。
销售数量:在中国销售数量为0
召回级别:ⅱ
20、上海上医康鸽医用器材有限责任公司
生产企业:上海上医康鸽医用器材有限责任公司
召回产品:部分灭菌后产品
召回原因:企业灭菌柜控制软件更新升级,灭菌参数做了调整,但企业未对灭菌过程进行再确认,不能保证灭菌产品无菌
销售数量:(点击查看大图)
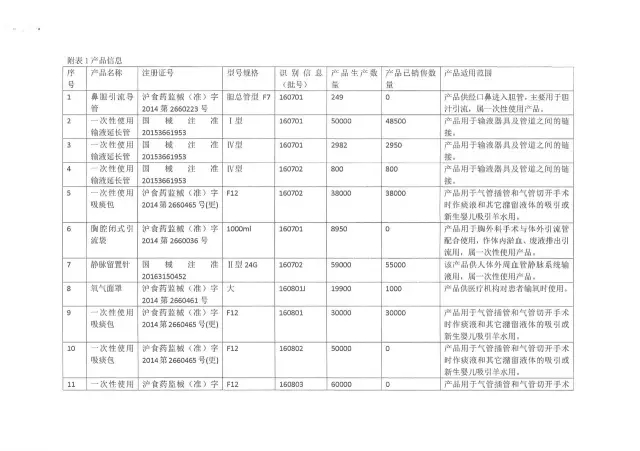
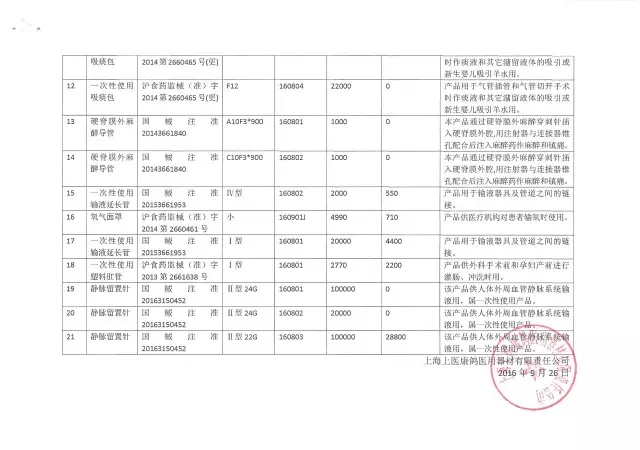
召回级别:ⅱ
【来源:医疗口碑整理自上海药监局】

相关阅读
- 10家医疗器械公司召回了过万件产品2018-10-31
- 关于医疗器械“召回” 你还应该了解这些2018-08-07
- 上海市医疗器械召回,国产数量在增多2018-07-25
- 一大波召回来袭 医疗器械召回新规发威了!2017-05-10
- 医疗器械召回管理办法落地 彻底影响械企!2017-05-02






