国家局责令两家械企立即停产整改! -凯发k8网页登录
近期,国家药品监督管理局组织对上海威宁整形制品有限公司、河南省豫北卫材有限公司进行了飞行检查。
飞检发现,两家企业生产质量管理体系均存在多项严重缺陷,国家药品监督管理局已责成上海市食品药品监督管理局、河南省食品药品监督管理局依法责令两企业立即停产整改。
待企业完成全部项目整改并经所在地省级食品药品监督管理局跟踪复查合格后方可恢复生产。
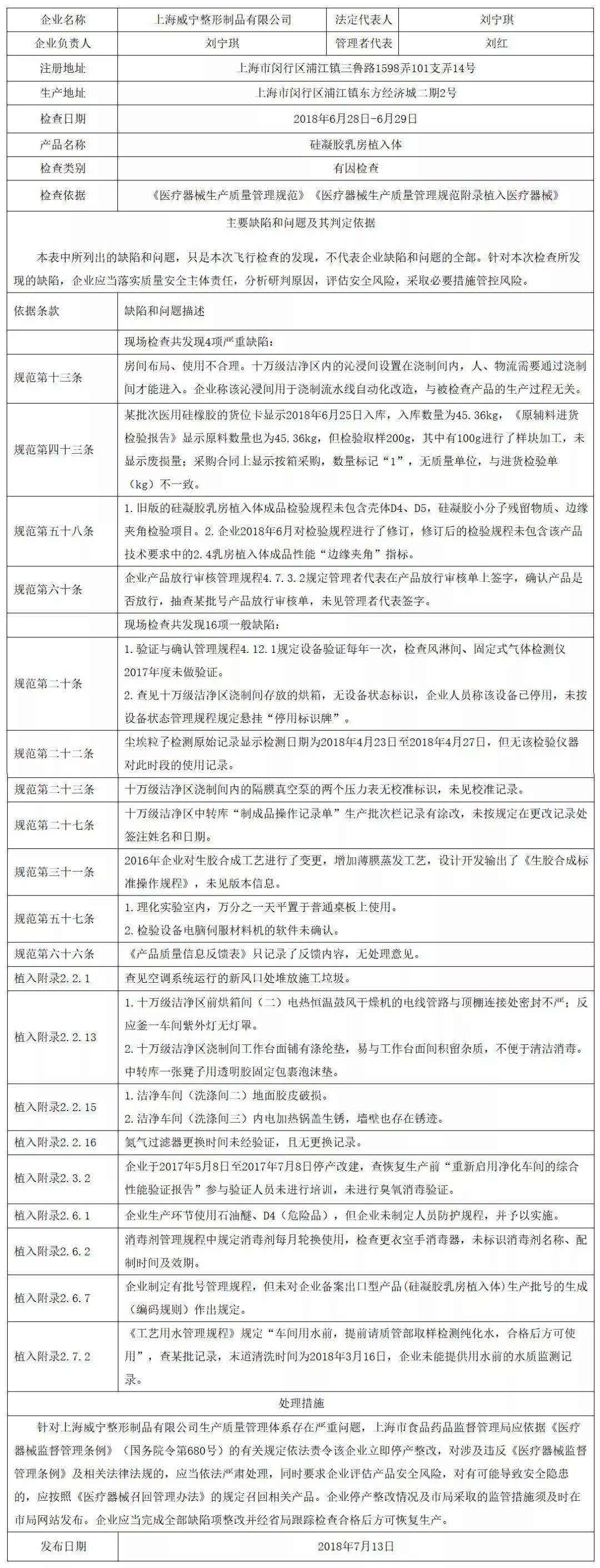
国家药品监督管理局关于上海威宁整形制品有限公司停产整改的通告
(2018年第61号)
一、厂房与设施方面
(一)企业房间布局、使用不合理,十万级洁净区内的沁浸间设置在浇制间内,人、物流需要通过浇制间才能进入,企业称该沁浸间用于浇制流水线自动化改造,与被检查产品的生产过程无关,不符合《医疗器械生产质量管理规范》及相关附录(以下简称《规范》)中厂房与设施应当根据所生产产品的特性、工艺流程及相应的洁净级别要求合理设计、布局和使用的要求。
(二)企业氮气过滤器更换时间未经验证,且无记录,不符合《规范》中与产品使用表面直接接触的气体,其对产品的影响程度应当进行验证和控制,以适应所生产产品的要求。
二、设备方面
企业于2017年5月8日至2017年7月8日停产改建,查恢复生产前“重新启用净化车间的综合性能验证报告”参与验证人员未进行培训,未进行臭氧消毒验证,不符合《规范》中若停机后再次开启空气净化系统,应当进行必要的测试或验证,以确认仍能达到规定的洁净度级别要求。
三、设计开发方面
2016年企业对生胶合成工艺进行变更,增加薄膜蒸发工艺,设计开发输出了《生胶合成标准操作规程》,输出清单未标注版本号,不符合《规范》中设计和开发输出应当得到批准,保持相关记录的要求。
四、采购方面
企业某批次医用硅橡胶的货位卡显示2018年6月25日入库,入库数量为45.36kg,《原辅料进货检验报告》显示原料数量也为45.36kg,但检验取样200g,其中有100g进行了样块加工,未显示废损量;采购合同上显示按箱采购,数量标记“1”,无质量单位,与进货检验单(kg)不一致,不符合《规范》中采购记录应当满足可追溯要求。
五、质量控制方面
(一)企业原检验规程未包含壳体d4、d5,硅凝胶小分子残留物质、边缘夹角检验项目,企业2018年6月对检验规程修订,修订后的检验规程未包含该产品技术要求的2.4乳房植入体成品性能“边缘夹角”指标,另硅凝胶乳房植入体成品检验规程规定壳体和硅凝胶中d4、d5项目每2年进行委托检验一次,硅凝胶乳房植入体过程检验规程规定硅凝胶d4、d5批批进行委托检验,不符合《规范》中企业应当根据强制性标准以及经注册或者备案的产品技术要求制定产品的检验规程,并出具相应的检验报告或者证书的要求。
(二)企业产品放行审核管理规程4.7.3.2规定管理者代表在产品放行审核单上签字,确认产品是否放行,抽查某批号产品放行审核单,未见管理者代表签字,不符合《规范》中企业应当规定产品放行程序、条件和放行批准要求。
(三)企业《工艺用水管理规程》规定“车间用水前,提前请质管部取样检测纯化水,合格后方可使用”,查某批记录,末道清洗时间为2018年3月16日,企业未能提供使用前的水质监测记录,不符合《规范》中应当对工艺用水进行监控和定期检测,并保持监控记录和检测报告的要求。
企业已对上述其质量管理体系存在缺陷予以确认。该企业上述行为不符合医疗器械生产质量管理规范相关规定,生产质量管理体系存在严重缺陷,国家药品监督管理局责成上海市食品药品监督管理局依法责令该企业立即停产整改,对涉及违反《医疗器械监督管理条例》(国务院令第680号)及相关法律法规的,依法严肃处理。同时责成上海市食品药品监督管理局要求该企业评估产品安全风险,对有可能导致安全隐患的,应按照《医疗器械召回管理办法》(国家食品药品监督管理总局令第29号)的规定,召回相关产品。
待企业完成全部项目整改并经所在地省级食品药品监督管理局跟踪复查合格后方可恢复生产。
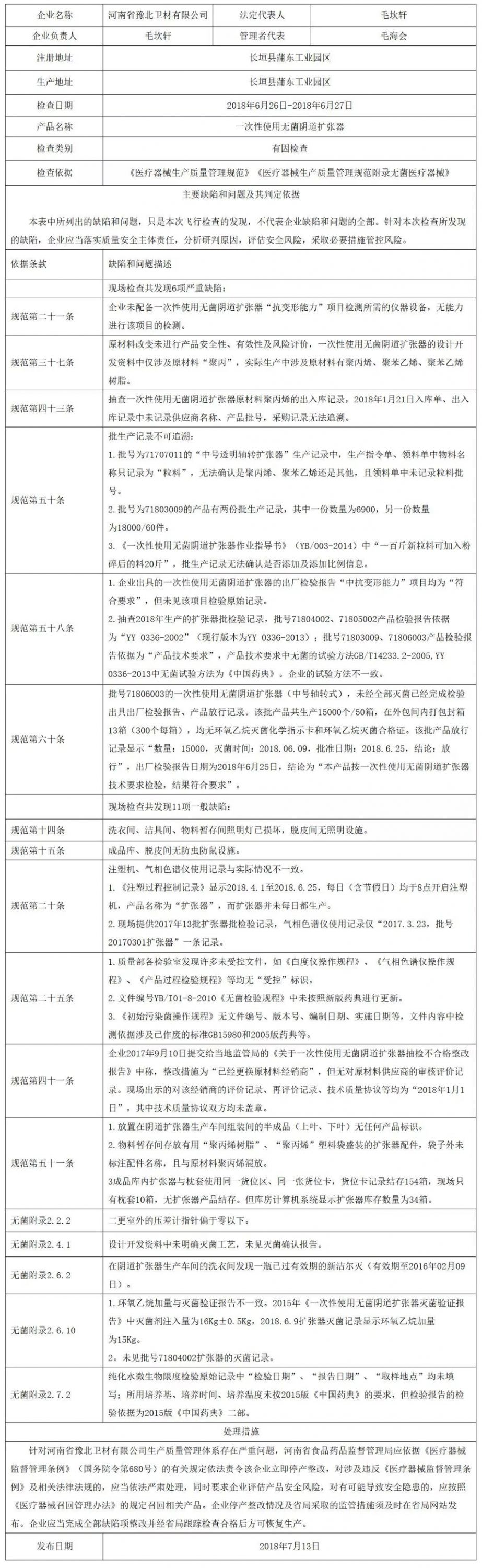
国家药品监督管理局关于河南省豫北卫材有限公司停产整改的通告
(2018年第62号)
近期,国家药品监督管理局组织对河南省豫北卫材有限公司进行了飞行检查。检查中,发现该企业质量管理体系主要存在以下缺陷:
一、厂房与设施方面
企业未配备一次性使用无菌阴道扩张器“抗变形能力”项目检测所需的仪器设备,无能力进行该项目的检测,不符合《医疗器械生产质量管理规范》及相关附录(以下简称《规范》)中企业应当配备与产品检验要求相适应的检验仪器和设备,主要检验仪器和设备应当具有明确的操作规程的要求。
二、设计开发方面
企业原材料改变未进行产品安全性、有效性及风险评价,一次性使用无菌阴道扩张器的设计开发资料中仅涉及原材料“聚丙”,实际生产中涉及原材料有聚丙烯、聚苯乙烯、聚苯乙烯树脂,不符合《规范》中当选用的材料、零件或者产品功能的改变可能影响到医疗器械产品安全性、有效性时,应当评价因改动可能带来的风险,必要时采取措施将风险降低到可接受水平,同时应当符合相关法规的要求。
三、采购方面
企业一次性使用无菌阴道扩张器采购的原材料聚丙烯,2018年1月21日入库单、出入库记录中未记录供应商名称、产品批号,采购记录无法追溯,不符合《规范》中采购记录应当满足可追溯要求。
四、生产管理方面
(一)企业批号71707011的中号透明轴转扩张器的生产记录中,生产指令单、领料单中物料名称只记录为“粒料”,无法确认是聚丙烯、聚苯乙烯还是其他,且领料单中未记录粒料批号,批号71803009的产品有两份批生产记录,一份数量为6900,一份为18000/60件,《一次性使用无菌阴道扩张器作业指导书》(yb/003—2014)中“一百斤新粒料可加入粉碎后的料20斤”,批生产记录无法确认是否添加及添加比例,不符合《规范》中每批(台)产品均应当有生产记录,并满足可追溯的要求。
(二)企业环氧乙烷加量与灭菌验证报告不一致。2015年《一次性使用无菌阴道扩张器灭菌验证报告》中灭菌剂注入量为16kg±0.5kg,2018.6.9扩张器灭菌记录显示环氧乙烷加量为15kg,未见批号71804002扩张器的灭菌记录,不符合《规范》中应当制定灭菌过程控制文件,保持每一灭菌批的灭菌过程参数记录,灭菌记录应当可追溯到产品的每一生产批的要求。
五、质量控制方面
(一)企业出具的一次性使用无菌阴道扩张器的出厂检验报告“抗变形能力”项目均为“符合要求”,未见该项目检验原始记录,抽查2018年生产扩张器批检验记录,批号71804002、71805002产品检验报告依据为“yy 0336—2002”(现行版本为yy 0336—2013),批号71803009、71806003产品检验报告依据为“产品技术要求”,产品技术要求中无菌的试验方法gb/t14233.2—2005,yy 0336—2013中无菌试验方法为《中国药典》,不符合《规范》企业应当根据强制性标准以及经注册或者备案的产品技术要求制定产品的检验规程,并出具相应的检验报告或者证书的要求。
(二)企业批号71806003的一次性使用无菌阴道扩张器(中号轴转式),未经全部灭菌已经完成检验出具出厂检验报告、产品放行记录,该批产品共生产15000个/50箱,在外包间内打包封箱13箱(300个每箱),均无环氧乙烷灭菌化学指示卡和环氧乙烷灭菌合格证,该批产品放行记录显示“数量:15000,灭菌时间:2018.06.09,批准日期:2018.6.25,结论:放行”,出厂检验报告日期为2018年6月25日,结论为“本产品按一次性使用无菌阴道扩张器技术要求检验,结果符合要求”,不符合《规范》中企业应当规定产品放行程序、条件和放行批准要求。
(三)纯化水微生物限度检验原始记录中“检验日期”“报告日期”“取样地点”均未填写,所用培养基、培养时间、培养温度未按2015版《中国药典》的要求,但检验报告的检验依据为2015版《中国药典》二部,不符合《规范》中应当对工艺用水进行监控和定期检测,并保持监控记录和检测报告的要求。
企业已对上述其质量管理体系存在缺陷予以确认。该企业上述行为不符合医疗器械生产质量管理规范相关规定,生产质量管理体系存在严重缺陷,国家药品监督管理局责成河南省食品药品监督管理局依法责令该企业立即停产整改,对涉及违反《医疗器械监督管理条例》(国务院令第680号)及相关法律法规的,依法严肃处理。同时责成河南省食品药品监督管理局要求该企业评估产品安全风险,对有可能导致安全隐患的,应按照《医疗器械召回管理办法》(国家食品药品监督管理总局令第29号)的规定,召回相关产品。
待企业完成全部项目整改并经所在地省级食品药品监督管理局跟踪复查合格后方可恢复生产。
附件:对上海威宁整形制品有限公司飞行检查通报
附件:对河南省豫北卫材有限公司飞行检查通报
【来源:国家药品监督管理局】







